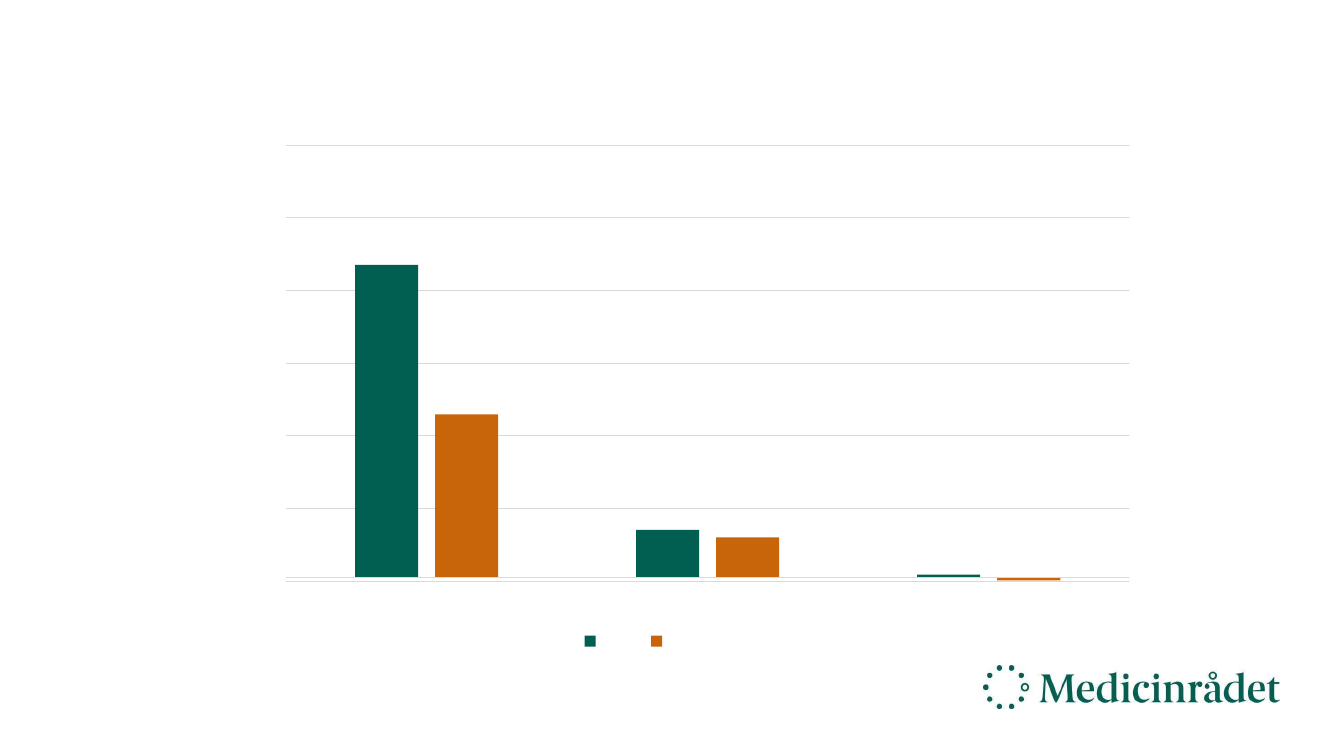Sundhedsudvalget 2020-21
SUU Alm.del Bilag 342
Offentligt
Møde med Folketingets Sundhedsudvalg
30. marts 2021
Teknisk gennemgang vedr. Medicinrådets metodeændring ift.
kategorisering af nye lægemidlers værdi, herunder betydning for
vurderingen af lægemidler til sjældne sygdomme
Jørgen Schøler Kristensen og Steen Werner Hansen, formænd for Medicinrådet
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Overblik over præsentationen
•
Medicinrådets formål
•
Metode til vurdering af nye lægemidler
•
Ændring af metoden per 1. januar 2019
•
Sjældne sygdomme
•
Metodeændringen og sjældne sygdomme
•
Omkostninger for lægemidler til sjældne og ikke-sjældne sygdomme
•
Ny metode i Medicinrådet per 1. januar 2021
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Medicinrådets formål
•
Medicinrådet er et uafhængigt råd nedsat af Danske
Regioner
•
Medicinrådet skal
•
sikre hurtig og ensartet ibrugtagning af nye sygehuslægemidler
•
stille større krav til dokumentation af lægemidlers effekt
•
sikre et stærkere grundlag for prisforhandlinger og udbud
Kilde: Medicinrådets kommissorium
3
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Medicinrådets formål
4
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Nye lægemidler/indikationsudvidelser
Medicinrådet har vurderet 128 lægemidler
som mulig standardbehandling på sygehusene
siden 1. januar 2017.
128 nye
lægemidler
Medicinrådet har yderligere udarbejdet:
•
25 behandlingsvejledninger
•
27 er på nuværende tidspunkt i proces
•
50 lægemiddelrekommandationer
Opdateret d. 26. marts
68 er blevet anbefalet
23 er blevet delvist anbefalet
37 er ikke blevet anbefalet
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
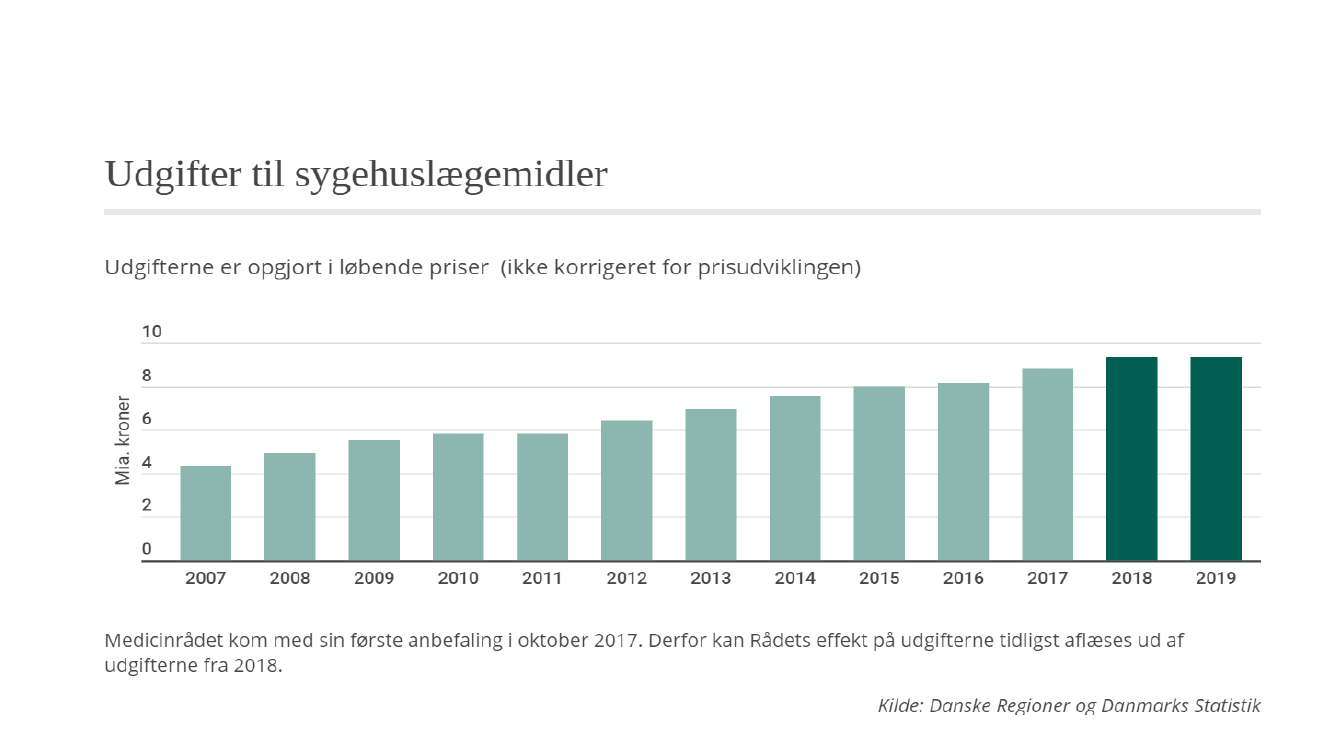
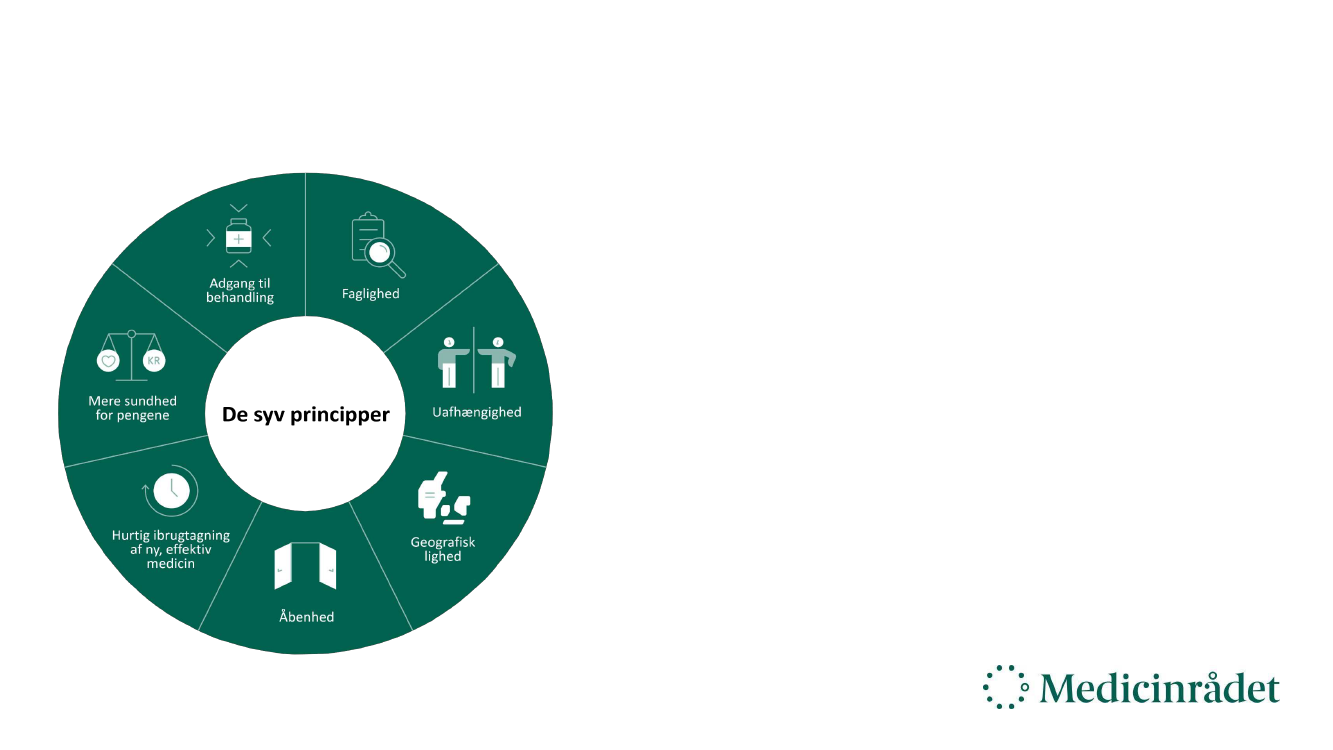
Folketingets syv principper for prioritering af sygehuslægemidler
De syv principper står ikke alene. Der er
yderligere to principper, som kan tages i brug:
Alvorlighedsprincippet:
Vi vil acceptere større
omkostninger hvis det er meget alvorlig
sygdom.
Forsigtighedsprincippet:
Vi vil ikke acceptere
væsentlige stigninger i samlede udgifter
grundet én behandling.
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Medicinrådets tidligere metode til vurdering af
lægemidlers værdi
Metode frem til 1. januar 2021:
•
Effekt og sikkerhed sammenlignes altid med den eksisterende behandling i
Danmark
•
Specifikke mål for effekt defineres i hver enkelt sag
•
Medicinrådet kategoriserer lægemidlets værdi ved at se på størrelsen på effekt (i
gennemsnit) og usikkerheden (herunder statistisk usikkerhed)
•
Metoden er inspireret af IQWIG i Tyskland
•
Per 1. januar 2021 er metoden ændret, så Medicinrådet fremover anvender
kvalitetsjusterede leveår (QALY)
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Metodeændringen 1. januar 2019
Formål og baggrund
•
Kriterierne for at kategorisere lægemidlers værdi var ikke præcise nok.
•
Metoden blev justeret i januar 2019 for at gøre kategoriseringen
mere præcis og skarpere
defineret
•
Målet var en
mere ensartet og transparent
vurdering af lægemidlers værdi
•
Metodeændringen var
ikke isoleret til lægemidler til sjældne sygdomme,
men generel for alle
lægemidler
•
Medicinrådet indførte muligheden for ikke at kategorisere lægemidlers værdi, hvis evidensen er
meget sparsom.
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Metodeændring 1. januar 2019
Tidligere metode (2017-2018)
1. Stor merværdi
2. Vigtig merværdi
3. Lille merværdi
Ændret metode (2019-2020)
Stor merværdi
Moderat merværdi
Lille merværdi
Merværdi af ukendt
størrelse
4. Ingen merværdi
5. Negativ merværdi
6. Ikkedokumenterbar merværdi
-
Ingen dokumenteret merværdi
Negativ værdi
-
Sa let værdi ”Ka ikke kategoriseres”
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Metodeændring 1. januar 2019
”Kan ikke kategoriseres”
•
Denne konklusion bruges, når datagrundlaget ikke entydigt viser, om lægemidlet er bedre eller ej
•
Når evidensen er meget sparsom, vurderer fagudvalget, om lægemidlet kan formodes at have en
bedre effekt end eksisterende behandling eller ej
•
Fagudvalget inddrager kliniske skøn og erfaringer i argumentationen
•
Medicinrådet havde forventet, at lægemidler til sjældne sygdomme ville være vanskelige at
kategorisere, fordi studierne af disse lægemidler ofte er meget små
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Hvad kendetegner sjældne sygdomme?
•
Der fi des ikke é klar defi itio af ”sjæld e sygdo
•
Sundhedsstyrelsen:
e”
•
mindre end 1-2 ud af 10.000, dvs. højst 500-1000 patienter i DK. Definitionen
dækker kun medfødte, arvelige, kroniske, komplekse, alvorlige sygdomme med
behov for en særlig indsats og faglige/teknologiske ressourcer. Dækker ikke kræft
og infektionssygdomme
•
EMA:
•
færre end 5 ud af 10.000, dvs. 2500 til 3000 i personer i DK
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Hvad kendetegner sjældne sygdomme?
Medicinrådets opdeling af lægemidler ift. sjældenhed
1. Lægemidler til sjældne sygdomme (jf. Sundhedsstyrelsens definition)
2. Lægemidler til sjældne kræftsygdomme (jf. fagudvalgets vurdering, < 50
patienter pr. år i Danmark)
3. Øvrige lægemidler (dvs. lægemidler som ikke opfylder definition 1 og 2)
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
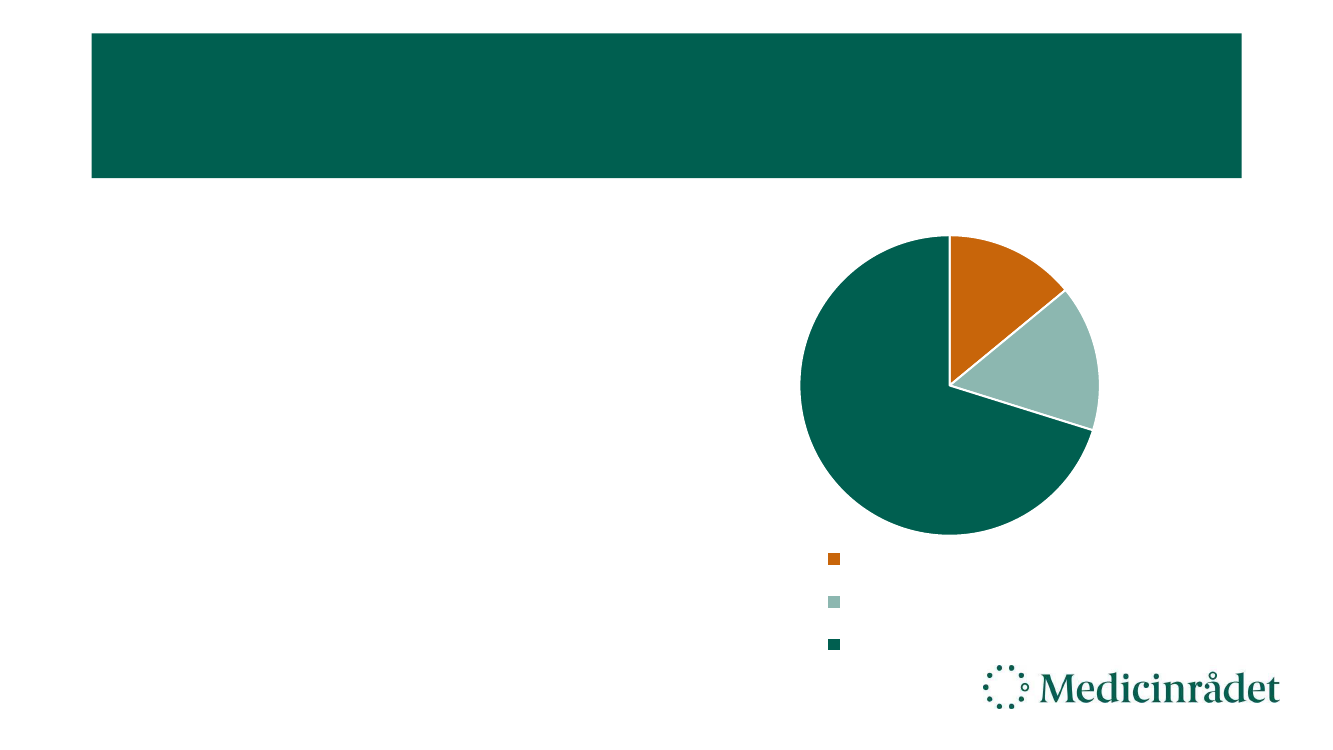
Hvor
ofte ser vi ”sjældent”?
Antal lægemidler fordelt på kategori
Per 18. november 2020 havde MR
vurderet 114 lægemidler:
•
16 var til sjældne sygdomme jf. SST definition
•
18 var til sjældne kræftsygdomme
(dvs. hvor FU estimerer <50 patienter om
året)
•
80 var ikke-sjældne sygdomme
Sjældne sygdomme
Sjældne kræftsygdomme
Ikke sjældne sygdomme
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Metodeændringen og sjældne sygdomme
•
Metodeændringens betydning for lægemidler til sjældne sygdomme blev analyseret i november
2020 - notat liger på vores hjemmeside
•
Opgørelsen viste at:
•
Alle
lægemidler til sjældne sygdomme kunne kategoriseres jf. den ændrede metode
•
1 stor merværdi, 3 moderat merværdi, 5 merværdi af ukendt størrelse
•
Lægemidler til sjældne kræftsygdomme
kan ofte ikke kategoriseres
(86 %)
•
1 lille merværdi, 1 merværdi af ukendt størrelse,
6
kan ikke kategoriseres
•
Anbefalinger efter metodeændringen
•
5 ud af 8 lægemidler til sjældne sygdomme er anbefalet eller delvist anbefalet
•
2 ud af 6 lægemidler til sjældne kræftsygdomme er anbefalet eller delvist anbefalet
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
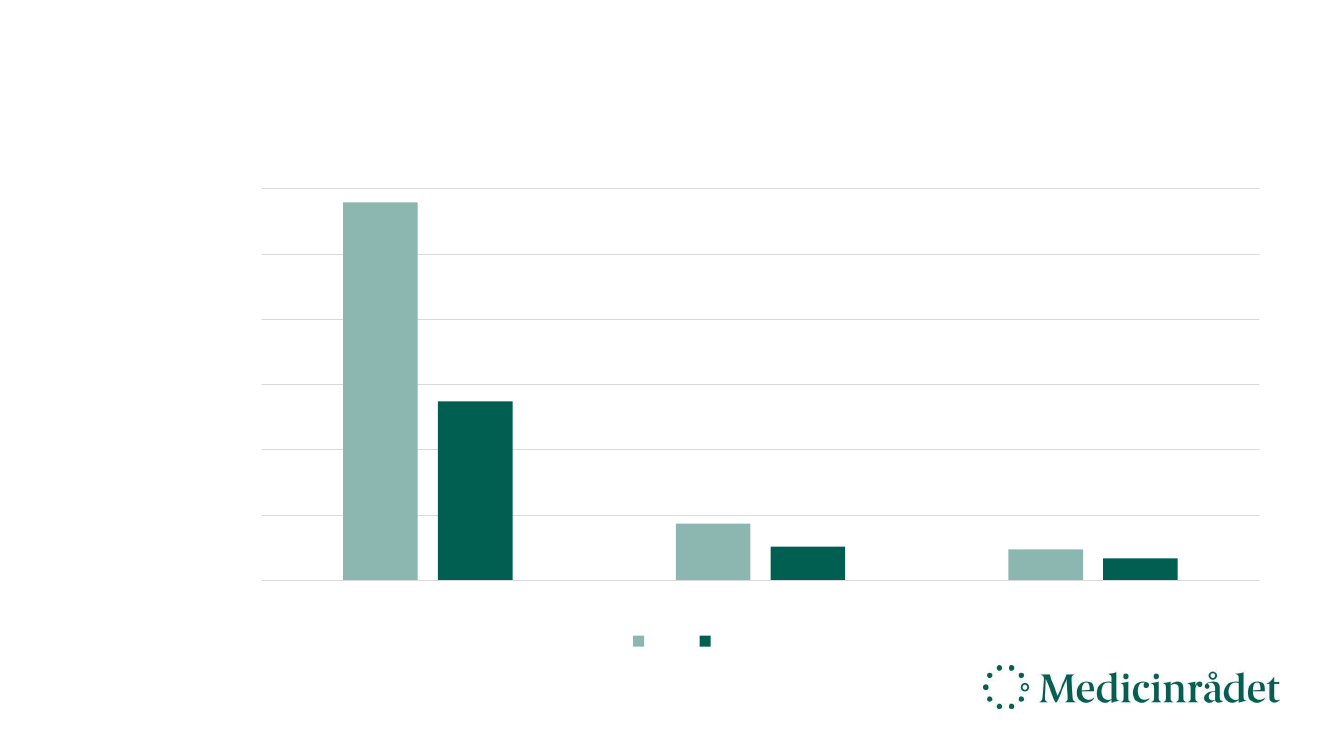
Gennemsnitlige meromkostninger (Alle ansøgninger)
5.950.000 kr.
5,0 mio. kr.
4.950.000 kr.
3.950.000 kr.
2.950.000 kr.
1.950.000 kr.
950.000 kr.
-50.000 kr.
2,5 mio. kr.
0,8 mio. kr.
0,5 mio. kr.
0,2 mio. kr. 0,1 mio. kr.
Resten
Sjældne sygdomme
Sjældne kræftsygdomme
AIP
SAIP
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
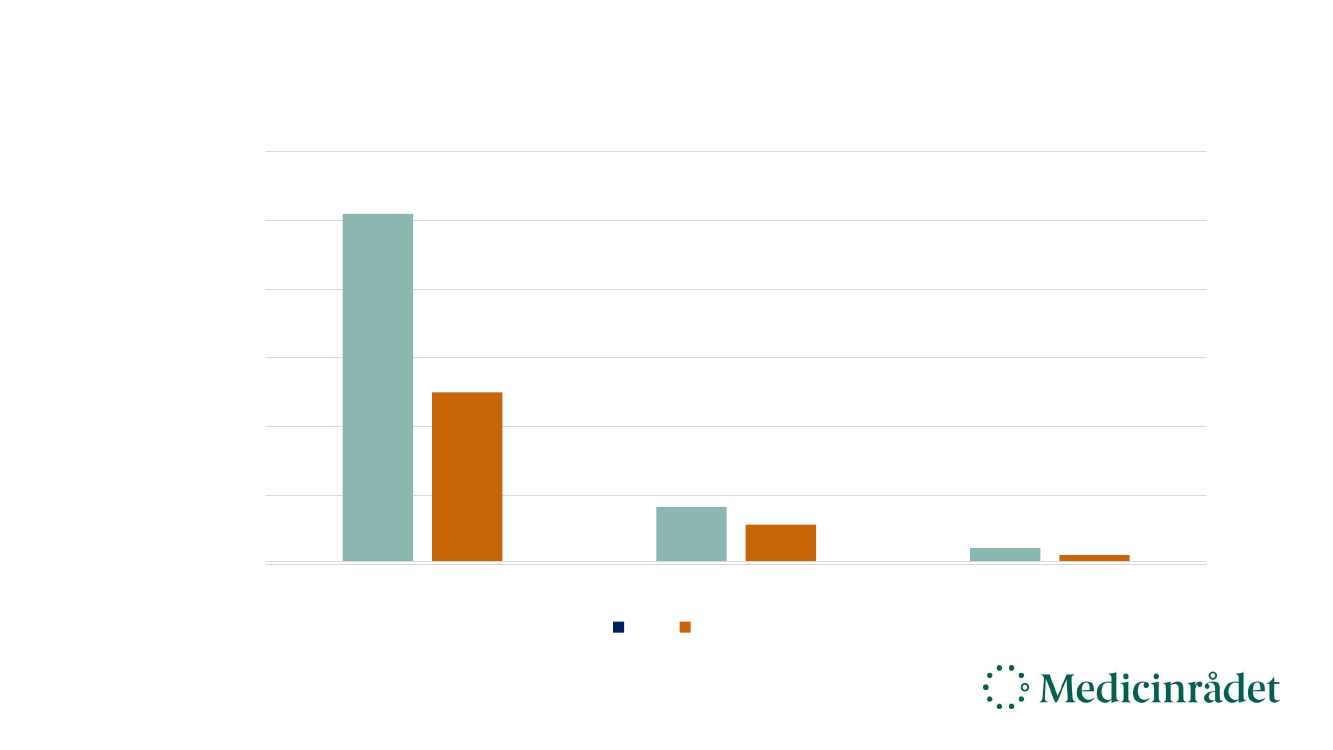
Gennemsnitlige meromkostninger (anbefalede lægemidler)
5.950.000 kr.
4.950.000 kr.
4,3 mio. kr.
3.950.000 kr.
2.950.000 kr.
2,2 mio. kr.
1.950.000 kr.
950.000 kr.
0,6 mio.
0,6 mio.
kr.
kr.
-0,03
0,05
mio. kr. mio. kr.
Resten
-50.000 kr.
Sjældne sygdomme
Sjældne kræftsygdomme
AIP
SAIP
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Gennemsnitlige meromkostninger (Ikke anbefalede lægemidler)
6.000.000 kr.
5.000.000 kr.
4.000.000 kr.
3.000.000 kr.
2.000.000 kr.
1.000.000 kr.
0 kr.
5,8 mio. kr.
2,7 mio. kr.
0,9 mio. kr.
0,5 mio. kr.
0,5 mio. kr.
0,4 mio. kr.
Sjældne sygdomme
Sjældne kræftsygdomme
AIP
SAIP
Resten
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Konklusioner vedr. omkostninger
•
Medicinrådet bidrager til markant priskonkurrence blandt lægemidler til ikke-sjældne
sygdomme
•
Forskellene på AIP og SAIP viser, at Medicinrådet og Amgros sikrer betydelige rabatter på nye
lægemidler
•
Lægemidler til sjældne sygdomme medfører markant højere omkostninger end andre
lægemidler
•
Medicinrådet anbefaler som regel lægemidler til sjældne sygdomme på trods af høje
omkostninger
•
Når Medicinrådet ikke anbefaler lægemidler skyldes det ofte, at der er usikkerheder om
effekten, som gør de høje omkostninger uacceptable
18
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Ny metode (QALY) 1. januar 2021
•
Medicinrådet er pr. 1/1-2021 overgået til en ny metode, hvor sundhedsgevinster opgøres i
kvalitetsjusterede leveår (QALY)
•
QALY ændrer ikke i sig selv på betydningen af usikkerheder
–
modellerne vil afspejle usikkerheder
i de kliniske studier
•
Der findes ikke en metode, som kan reducere de grundlæggende usikkerheder i evidensen
•
Vi håber dog, at vi med modellerne bedre kan undersøge betydningen af usikkerheder for QALY-
estimatet, og herved kvalificere Rådets diskussioner og beslutninger
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Konklusioner
•
Medicinrådet opdaterede metoden for at sikre ensartethed i kategoriseringer
på tværs af lægemidler
•
Lægemidler til sjældne sygdomme kan oftest kategoriseres på trods af, at vi
skærpede kravene til dokumentationen ved metodeændringen
•
Lægemidler til sjældne kræftsygdomme kan ofte ikke kategoriseres på grund
af begrænsninger i datagrundlaget
•
Medicinrådet inddrager altid både effekt, sikkerhed og omkostninger i den
samlede vurdering af, om lægemidler skal anbefales som standardbehandling
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Konklusioner
•
Medicinrådet anbefaler ofte lægemidler til sjældne sygdomme, på trods af
markant højere omkostninger for disse lægemidler
•
Medicinrådet er skiftet til ny metode per 1. januar 2021, hvor effekt måles i
kvalitetsjusterede leveår (QALY)
•
Vi vil se et stigende antal lægemidler til små undergrupper af kræftsygdomme
i fremtiden. Det er især her vi har udfordringer med meget sparsomme data
•
Vi forventer også at se flere lægemidler til sjældne sygdomme (ikke-kræft)
•
Forekomsten af sager med sparsomme data og høje omkostninger forventes
at være stigende i fremtiden
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
SPØRGSMÅL
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
EKSTRA SLIDES
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
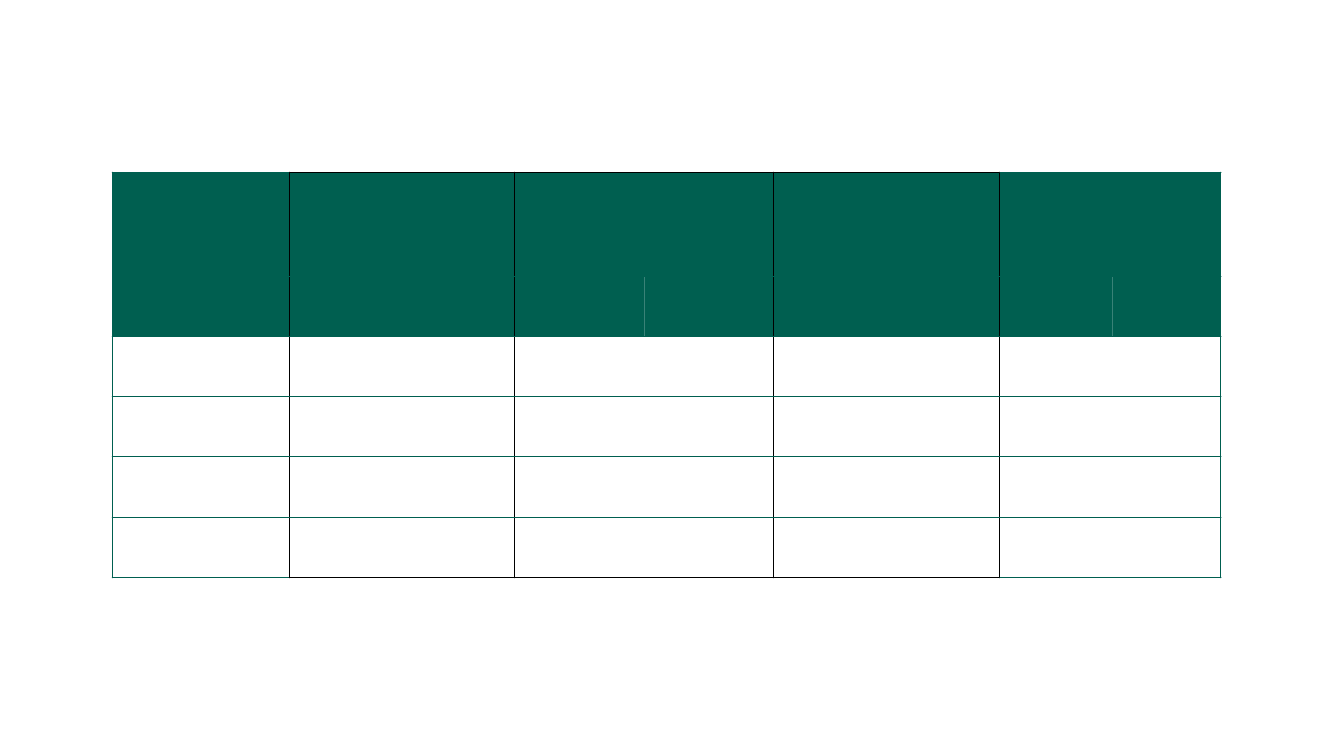
Oversigt over anbefalinger før og efter metodeændringen
Anbefalinger i alt
(114 lægemidler)
Tidligere
metoder
Sjældne
sygdomme
Sjældne kræft-
sygdomme
Øvrige sygdomme
Alle lægemidler
10
13
49
72
Ændret
metode
6
5
31
42
’Anbefalet’
Tidligere
metoder
4
(40 %)
9
(69 %)
Ændret
metode
4
(67 %)
1
(20 %)
’Delvist anbefalet’
Tidligere
metode
3
(30 %)
0
(0 %)
Ændret
metode
1
(17 %)
0
(0 %)
’Ikke anbefalet’
Tidligere
metode
3
(30 %)
4
(31 %)
Ændret
metode
1
(17 %)
4
(80 %)
27
(55 %)
40
(56 %)
17
(59 %)
21
(52 %)
10
(20 %)
13
(18 %)
4
(13 %)
4
(10 %)
12
(24 %)
19
(26 %)
10
(32 %)
15
(38 %)
(Tallene er opgjort 18. november 2020)
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Alvorlighedsprincippet
Alvorlighedsprincippet er pr. 18.11.20
blevet brugt i 7 sager
Antal sager, hvor alvorlighedsprincippet er
benyttet fordelt på kategori
•
2 gange i sager, der ikke er defineret som
”sjæld e sygdo
e” eller sjælde kræft
•
2 gange til sjældne kræftformer (< 50 ptt om året i DK)
•
3 gange til sjældne sygdomme (jf. SST definition)
Ikke sjældne sygdomme
Sjældne kræftsygdomme
Sjældne sygdomme
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Udfordringer som særligt har betydning for
Medicinrådets arbejde
•
Patientgruppen er typisk meget lille, eventuelt heterogen
•
Det kan være vanskeligt at udføre kliniske studier med tilstrækkelig styrke og lang nok
opfølgningstid
•
Der er få danske kliniske eksperter
•
Lægemidlerne er ofte markant dyrere end lægemidler til mere almindelige sygdomme
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Den generelle viden om sygdommene kan være
begrænset
•
Der kan være begrænset viden om sygdommens spontanforløb og karakteristika i den
videnskabelige litteratur
•
Der kan være meget begrænset erfaring med behandling i Danmark
•
Det kan give udfordringer i Medicinrådets arbejde, når kliniske studier skal tolkes og
anvendeligheden af sundhedsøkonomiske modeller skal vurderes
•
Derfor spiller fagudvalgene og deres erfaringsbaserede vurderinger en meget vigtig rolle ved
vurderingen af disse lægemidler
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
De kliniske studier har ofte begrænsninger
•
Antallet af inkluderede patienter kan være meget begrænset
•
Opfølgningstiden i studierne er ofte begrænset, mens sygdommene ofte udvikler sig
over mange år
•
Effektmål - Der kan mangle validerede effektmål som fagudvalget har kendskab til.
Ved surrogatmål kan der mangle evidens for korrelation til direkte effektmål
(dødelighed og overlevelse)
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Medicinrådets arbejde med sjældne sygdomme
•
Afvejning mellem effekt og omkostninger
•
Effekten er ofte usikker, især langtidseffekter og hårde endepunkter
•
Når der er meget sparsom evidens, baseres de samlede vurderinger af effekt i høj grad på de vurderinger som
fagudvalgenes kliniske eksperter foretager
•
Prisen kan være meget høj
•
Ud fra en konkret vurdering kan alvorlighedsprincippet tages i anvendelse
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Implementering af QALY og Medicinrådets nye
metodevejledning
•
Lægemidler til sjældne sygdomme skal vurderes ud fra samme metodiske ramme som andre lægemidler
•
Der findes ikke en metode som kan fjerne usikkerheder i datagrundlaget og derved gøre Medicinrådet
mere sikker i sine vurderinger, når der skal træffes beslutning om anbefaling
•
Derfor spiller fagudvalgene også fortsat en stor rolle når Medicinrådet skal vurdere lægemidler
•
Medicinrådet kan fortsat bruge alvorlighedsprincippet og vil stadig foretage en konkret vurdering af, om
usikkerhederne er acceptable, når effektstørrelser og omkostninger tages i betragtning
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Folketingets syv principper for prioritering af sygehuslægemidler
Faglighed:
Ved vurdering af lægemidler skal der
ske en grundig og systematisk vurdering af den
behandlingsmæssige gevinst for patienterne samt
den dokumentation, der ligger til grund herfor. Ved
vurderingen af lægemidler skal der inddrages den
nødvendige og tilstrækkelige faglige ekspertise.
Yderligere principper:
alvorlighed og forsigtighed
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Folketingets syv principper for prioritering af sygehuslægemidler
Uafhængighed:
Vurdering af lægemidler skal
ske ud fra objektive kriterier og på baggrund af
faglige vurderinger, således at der sikres et
uafhængigt udarbejdet beslutningsgrundlag og
derved armslængde til det politiske niveau.
Yderligere principper:
alvorlighed og forsigtighed
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Folketingets syv principper for prioritering af sygehuslægemidler
Geografisk lighed:
Der skal ske en ensartet
ibrugtagning og anvendelse af lægemidler på
tværs af hele landet. Der skal desuden være
entydighed i, hvordan de forskellige regioner
og sygehuse håndterer de tilfælde, hvor
lægemidler afvises til ibrugtagning som
standardbehandling.
Yderligere principper:
alvorlighed og forsigtighed
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Folketingets syv principper for prioritering af sygehuslægemidler
Åbenhed:
Der skal være størst mulig åbenhed
i vurderingen af lægemidler. Dvs. at der skal
være åbenhed om både processer, metoder,
kriterier og det materiale, der udarbejdes i
forbindelse med vurderingen af lægemidler.
Det skal således være muligt for alle at se
grundlaget og begrundelserne for at til- eller
fravælge nye lægemidler, jf. også
Transparensdirektivets krav i forhold til
objektivitet og gennemsigtighed. Åbenheden
har også til formål at facilitere en offentlig
debat.
Yderligere principper:
alvorlighed og forsigtighed
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Folketingets syv principper for prioritering af sygehuslægemidler
Hurtig ibrugtagning af ny, effektiv medicin:
Patienter skal have gavn af
behandlingsmæssige fremskridt. Danmark skal
fortsat være et af de lande, der hurtigst
ibrugtager nye lægemidler, hvor der er
dokumenteret mereffekt.
Yderligere principper:
alvorlighed og forsigtighed
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Folketingets syv principper for prioritering af sygehuslægemidler
Mere sundhed for pengene:
Midlerne i
sundhedsvæsenet, herunder til sygehuslægemidler,
skal bruges med omtanke, da det ellers kan få
konsekvenser for forebyggelse, behandling eller
pleje i andre dele af sundhedsvæsenet. Nye
lægemidler, som har en veldokumenteret mereffekt
skal ikke afvises alene på grund af økonomi.
Såfremt et nyt lægemiddel skal være
standardbehandling, skal der således være et
rimeligt forhold mellem prisen på det nye
lægemiddel og den merværdi, som lægemidlet
vurderes at kunne tilbyde sammenlignet med
eksisterende standardbehandling.
Yderligere principper:
alvorlighed og forsigtighed
SUU, Alm.del - 2020-21 - Bilag 342: Præsentation fra møde med sundhedsministeren og Medicinrådet 6/4-21 om rådets metodeændring for kategorisering af nye lægemidlers værdi
Folketingets syv principper for prioritering af sygehuslægemidler
Adgang til behandling:
Der skal sikres lige adgang
for både store og små patientgrupper og tages højde
for patienters individuelle behov. Det skal være
muligt ud fra en konkret lægefaglig vurdering at
behandle med lægemidler, som er afvist til
standardbehandling. Det gælder eksempelvis i
forhold til at kunne yde behandling af høj kvalitet
til patienter med sjældne sygdomme eller i forhold
til at kunne behandle for at undgå
funktionsnedsættelse.
Yderligere principper:
alvorlighed og forsigtighed